最近,药学院叶文才教授、王磊研究员团队与南方科技大学李闯创教授合作,在化学顶级期刊《Journal of the American Chemical Society》(IF: 14.61)发表题为“Asymmetric Total Synthesis of Bufospirostenin A”的研究论文,首次完成了复杂天然产物Bufospirostenin A的不对称全合成。我院博士研究生程民井和南方科技大学博士研究生钟李平为共同第一作者,李闯创教授、叶文才教授、王磊研究员为共同通讯作者,暨南大学为第一通讯单位。
天然化合物是创新药物的重要源泉,然而,天然化合物的分离量有限,制约了其进一步深入研究。Bufospirostenin A (1) 是我院研究团队从中华大蟾蜍中分离得到的新颖结构甾体化合物,具有复杂5/7/6/5/5/6六环骨架及11个手性中心(包括10个连续手性中心) (图1)。5/7/6/5骨架也存在于其他天然产物中(如2-5,图1),目前尚无该类骨架的全合成报道。
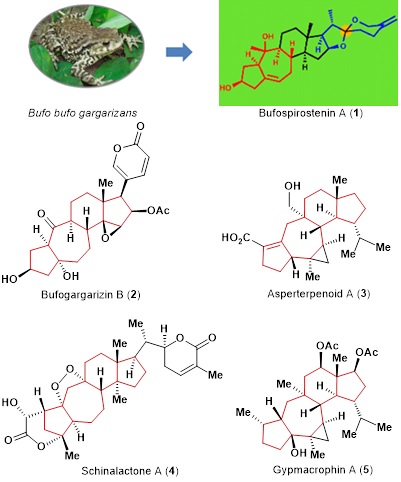
图 1. 天然产物Bufospirostenin A (1) 和其他含5/7/6/5四环骨架(红色标记) 的天然产物结构。(图片来源于J. Nat. Prod. 2017, 80, 1182−1186和JACS doi/10.1021/jacs.0c05479)。
作者从易得的手性原料10出发,经过5步转化制备烷氧基联烯-炔Pauson–Khand反应前体9。接着,在 [RhCl(CO)2]2 催化作用下,发生分子内Pauson–Khand反应得到含5/7/6/5四环核心骨架的8 (绝对构型由单晶X-射线衍射分析证实,2步产率85%) (图2)。值得注意的是,富电子烷氧基联烯结构不稳定,分子内含有裸露的羟基,同时存在不利于关环的热力学熵变,这些因素使得上述Pauson–Khand反应的发生具有较大挑战。化合物8经过一系列的反应包括消除反应、氧化还原反应、增碳反应等,得到内酯25。最后,化合物25在SOCl2/Py.条件下消除叔醇羟基,并经过1,2-加成反应,以及半缩酮反应顺利完成天然产物Bufospirostenin A (1)的不对称全合成(图3)。通过活性筛选,发现该化合物具有显著的抗炎活性。

图2. 化合物19的不对称合成。图片来源:JACS
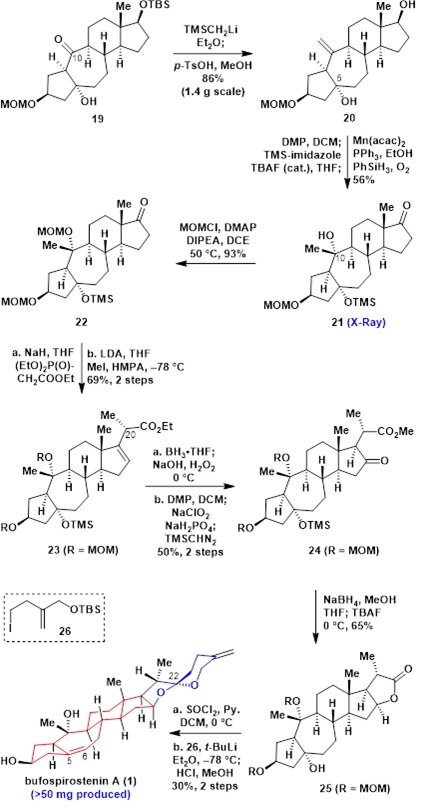
图3. Bufospirostenin A (1) 的不对称合成。图片来源:JACS
综上所述,该论文首次采用分子内烷氧基联烯-炔Pauson-Khand反应高效构建5/7/6/5四环骨架,经过20步完成了Bufospirostenin A的首次不对称全合成,并立体选择性的构建了11个手性中心。
该合成策略为后续其它类似天然化合物的不对称合成提供了范例。
论文链接:https://pubs.acs.org/doi/10.1021/jacs.0c05479







